Isotope analysis
同位体分析手法について、各元素の特徴やデータの解釈における注意点などを解説します。誤りやコメントがございましたら、matsu-jun@jamstec.go.jpまでご連絡よろしくお願いします。
同位体とは
同位体
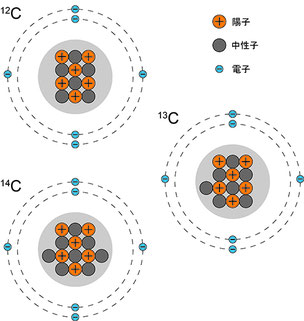
同じ原子番号(陽子数)で、中性子数が異なる原子を同位体といいます。例えば炭素では、天然に存在するものでは12C、13C、14Cの3種類の同位体が存在します。
安定同位体と放射性同位体
同位体のうち、時間経過に伴って放射壊変を起こすものを放射性同位体と呼び、時間的に常に安定なものを安定同位体と呼びます。炭素では、12C、13Cが安定同位体、14Cが放射性同位体です。
同位体の存在比(同位体比)
同位体の存在比
軽い同位体に対する重い同位体の比を、同位体比と呼びます。一般的に、軽い同位体の存在比は、重い同位体に比べて極端に高くなっています。例えば、天然に存在する炭素では、質量数12の同位体が98.93%なのに対して、質量数13の炭素は1.07%しか存在しません。
同位体比
同位体の組成について記述する際には、軽い同位体の存在比に対する重い同位体の存在比(=同位体比)が用いられます。例えば、質量数13の炭素の安定同位体比は、13C/12Cで算出されます。ここで、13Cは質量数13の炭素の存在比、12Cは質量数12の炭素の存在比を示します。

δ(デルタ)表記法
δ値
一般的に重い同位体の存在比は、軽い同位体の存在比に比べて極めて小さくなります。そのため、単純な同位体比では同位体組成の変動が分かりにくい場合があります。そこで、同位体比を記述する際には、国際的な標準試料の同位体比を基準として、それに対する測定試料の同位体比の千分偏差(‰)で表す場合があります。これは、δ表記法と呼ばれます。

δ表記法の定義
同位体比をδ標記法で表す場合、論文ごとにその定義法を記載する必要があります。右に示したのは、δ値の定義式の例です。定義式の書き方を統一するためのガイドラインがCoplen(2011)に示されています。混乱を避けるため、図の一番上のような定義式を使用することが推奨されています。

Coplen, TB. (2011) Guidelines and recommended terms for expression of stable isotope-ratio and gas-ratio measurement results. Rapid Commun. Mass Spectrom. 2011, 25, 2538–2560.
論文で同位体比を記載するときの注意事項
論文等で同位体比を扱う場合の記載方法に関するガイドラインがIUPACのCIAAWにより示されています。具体的な注意事項がBond and Hobson (2012)にまとめられています(下図)。
Equiation 1は、上のδ表記法の定義式のEquation 1を示しています。有効数字の行の理由の()内の記載は僕の私見です。

Bond, A.L., & Hobson, K.A. (2012) Reporting stable-isotope ratios in ecology: recommended terminology, guidelines and best practices. Waterbirds, 35, 324-331.